多重微珠流式免疫荧光法检测自身抗体
自身抗体测定在自身免疫病诊断及鉴别诊断中具有重要作用。因此,早期检测自身抗体是筛查自身免疫性疾病的重要举措[1]。你知道目前实验室有哪些检测方法吗?目前,检测方法主要有间接免疫荧光法[2]、免疫印迹法和ELISA[3]、[4]等,今天给大家介绍一种自身抗体测定新方法新技术——多重微球流式荧光免疫技术。
随着自免检测技术的不断发展,国外的液相芯片技术发展迅速且日益成熟,Luminex 公司[5]-[7]等已形成多色编码微球检测,相比国内,该技术仍处于初步阶段,是一项尚未完全发挥全部价值的技术。多重微球流式荧光免疫技术是一种以荧光编码微球为核心,集流式细胞、激光分析、高速数字信号处理等多种技术于一体的多指标并行分析技术平台,通量高,灵活组合,可一次同时准确定量检测100种不同的生物分子,高度自动化、稳定性好等优点,有文献报道该检测方法能弥补传统方法的弊端[8]。

多重微珠流式免疫荧光法检测自身抗体项目:
可灵活选择抗核抗体谱检测项目,包括抗组蛋白抗体,抗着丝点抗体,抗U1-RNP抗体,抗Sm抗体,抗SSA抗体,抗SSB抗体,抗Scl-70抗体,抗Jo-1抗体,抗dsDNA抗体等等。

图1:雅典娜流式荧光诊断系统

多重微珠流式免疫荧光法检测原理
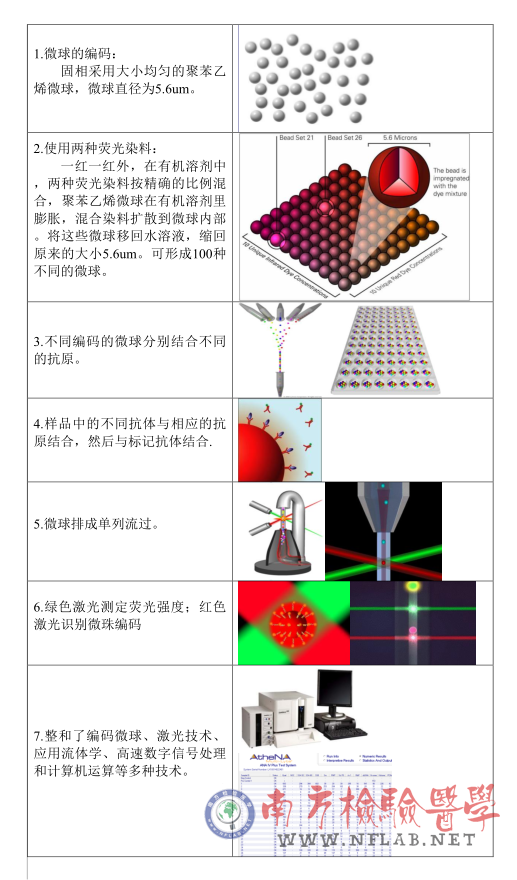

实验步骤
经过稀释的待测血清与复合悬浮微珠在孔中温育。复合悬浮微珠为不同荧光编码的聚苯乙烯微粒;不同颜色的微粒上结合有不同的抗原。如果血清中含有自身抗体,一种或多种自身抗体就会分别和不同颜色的微粒特异性地结合,温育30±10分钟后清洗微球。
加入荧光标记的羊抗人IgG 温育。标记抗体通过上一步反应固定在微粒表面的自身抗体结合。用AtheNA Multi-Lyte®系统(Luminex®仪器)对微粒悬浮液进行分析。仪器可以辨认出不同颜色的微粒,并测量出每个颗粒上的荧光强度。利用孔内校正技术,内对照颗粒上的荧光信号可以将读到的荧光强度转换成浓度结果。
检测结果判断标准:阴性样本<100AU/mL;阳性样本>120 AU/mL;临界值样本,100-120 AU/mL。

性能特点
2
高通量
一个检测孔同时检测多个指标。
2
全定量结果
有助于病情监测和指导临床用药。
2
定量动态诊断
疾病是动态发展变化的,定量诊断是一个动态的诊断过程,可以反映出疾病的发展变化状况。通过动态分析指标,可以给临床提供更加合理的诊断建议。
2
内定标技术-特异性高
为了消除基质效应,排除干扰。
2
灵敏度高 线性范围广
2
重复性好
每项检测结果都来自于至少50个微球结果的中位值
2
均相反应—反应更充分
2
高稳定性
检测板相当于反应杯,未包被任何物质。
2
用于快速自免检测多重微珠流式免疫荧光法检测时间90min
综上所述,多重微珠流式免疫荧光技术具有快速、定量和实时数据分析等优点,因而在免疫分析领域中具有应用价值,可以为临床医师诊断相关自身免疫性疾病、确定治疗方案及判断预后提供有力的实验室依据。
[1] 刘玉枝, 代荣琴, 陈洋,等. 自身抗体对系统性红斑狼疮的诊断价值[J]. 热带医学杂志, 2016, 16(1):39-41.
[2] Venrooij W, Charles P, Maini R N. The consensus workshops for the detection of autoantibodies to intracellular antigens in rheumatic diseases[J]. Clinical & Experimental Rheumatology, 1992, 10(5):507.
[3] Emlen W, O'Neill L. Clinical significance of antinuclear antibodies: comparison of detection with immunofluorescence and enzyme-linked immunosorbent assays[J]. Arthritis & Rheumatology, 2010, 40(9): 1612-1618.
[4] Froelich C J, Wallman J, Skosey J L, et al. Clinical value of an integrated ELISA system for the detection of 6 autoantibodies (ssDNA, dsDNA, Sm, RNP/Sm, SSA, and SSB).[J]. Journal of Rheumatology, 1990, 17(2): 192-200.
[5] Li W , Zhang N , Gong P , et al. A novel multiplex PCR coupled with Luminex assay for the simultaneous detection of Cryptosporidium spp. Cryptosporidium parvum and Giardia duodenalis[J]. Veterinary Parasitology, 2010, 173(1):11-18.
[6] Anderson S , Wakeley P , WiBbErley G , et al. Development and evaluation of a Luminex multiplex serology assay to detect antibodies to bovine herpes virus 1, parainfluenza 3 virus, bovine viral diarrhoea virus, and bovine respiratory syncytial virus, with comparison to existing ELISA detection methods[J]. Journal of Immunological Methods, 2011, 366(1-2):79-88.
[7] Grangeot-Keros V . PX-2 Evaluation of new multiplex assays for the BioPlex™ 2200 (Bio-Rad): preferential Toxoplasma gondii and cytomegalovirus IgM response for recently acquired infections[J]. Journal of Clinical Virology, 2009. 46:548.
[8] 胡朝军, 李永哲, 张蜀澜,等. AtheNA Multi-Lyte自身抗体自动化检测系统检测抗核抗体的性能评价[J]. 临床检验杂志, 2006, 24(005):387-388.
